
2025年12月11日,Journal of Advanced Research期刊(5年IF=11.6,综合性1区Top期刊)在线发表了山东大学微生物改造技术全国重点实验室王海龙教授课题组的研究论文“Combinatorial genome engineering of pseudorabies virus Bartha by developing a reverse genetic system based on three overlapping genomic segments”。 王海龙教授为论文通讯作者,博士后袁恒星、博士生张雨璐和已毕业硕士生谭龙为共同第一作者。山东大学微生物改造技术全国重点实验室为第一完成单位和通讯作者单位。

伪狂犬病病毒(Pseudorabies virus,PRV)Bartha 株是天然减毒的 α 疱疹病毒毒株,作为防控猪伪狂犬病的减毒活疫苗已在全球范围内广泛应用60 余年。因安全性高、免疫原性强等特性,Bartha在载体疫苗和溶瘤病毒研发领域也展现出独特且重要的价值。Bartha基因组为138 kb的双链 DNA,理论上可容纳15 kb 的外源基因片段,远高于腺病毒等常见载体,能同时装载多个病原的保护性抗原基因(如多价疫苗),或融合免疫调节因子(如细胞因子、佐剂基因)以增强免疫效果。充分发掘Bartha作为疫苗载体和溶瘤病毒的潜力,需要开发高效基因组编辑技术和系统鉴定其基因组上的非必需基因。
为了实现Bartha基因组的高效、多位点同时基因编辑,该研究将138 kb 的Bartha 基因组拆分为三个相互重叠的片段(42 kb、43 kb 和 53 kb),每个片段均被克隆至细菌人工染色体(BAC)中。将从 BAC 中释放的 3 个基因组片段转染至非洲绿猴肾细胞(Vero 细胞)后,相邻片段可借助 2 kb 的重叠区域完成完整病毒基因组的组装,进而实现感染性病毒的拯救。
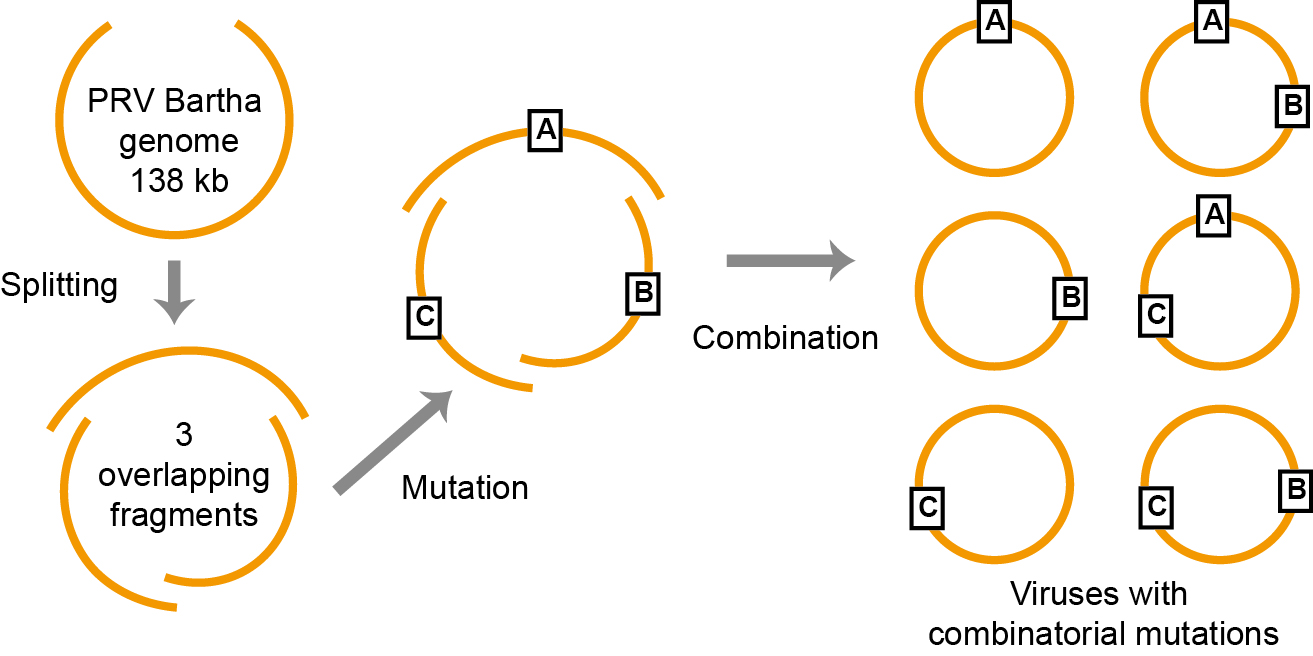
图1 伪狂犬病病毒Bartha疫苗株基因组的高效多位点基因编辑体系
利用上述反向遗传系统,该研究对 15 个候选非必需基因进行了单独敲除,证实其中 10 个基因在细胞培养体系中对Bartha病毒增殖是非必需的。其中,7 个非必需基因的敲除未对病毒增殖造成显著影响;UL44或 US3 基因的敲除会导致病毒噬斑变小,但不改变病毒增殖速率;UL47 基因的敲除既会导致病毒噬斑变小,还会降低病毒增殖速率。该研究共构建了 45 个非必需基因双敲除的Bartha病毒基因组,其中 22个成功被拯救为具有感染性的病毒颗粒。15 株双敲除突变体病毒的滴度与野生型 Bartha 株相当,其余 7 株的滴度则有所下降。此外,该研究还对10个非必需基因位点处 mNeonGreen 报告基因的表达情况进行了评估:在 8 个位点插入 mNeonGreen构建的重组病毒感染细胞后,可观察到强烈的绿色荧光;而在 2 个位点插入该报告基因构建的重组病毒感染细胞后,仅能检测到极微弱的荧光。
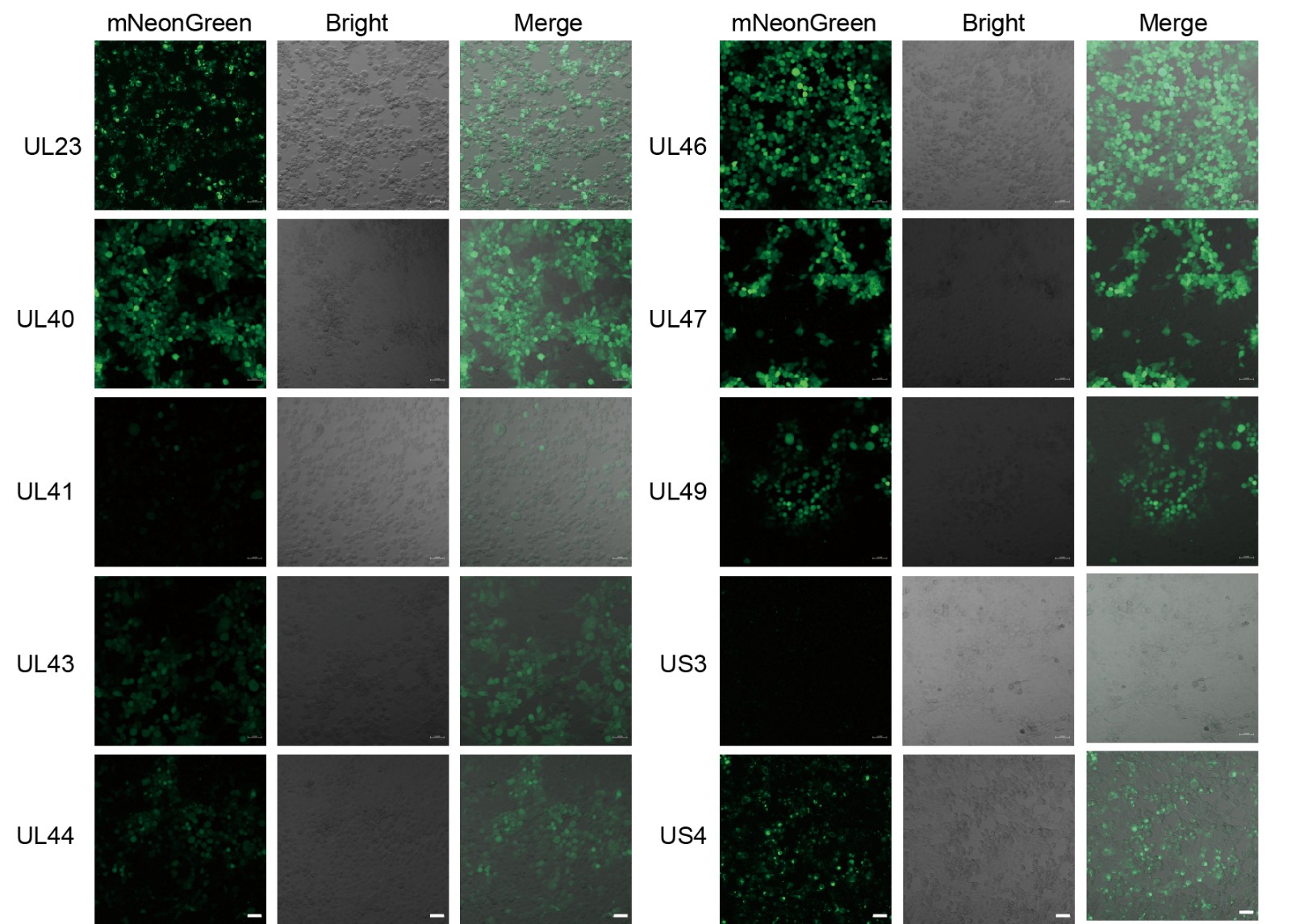
图2 Bartha基因组非必需位点的mNeonGreen报告基因表达情况
本研究建立的反向遗传系统可实现大基因组DNA病毒的快速组合式工程改造,这将加速基于大基因组DNA病毒的治疗技术研发,包括减毒活疫苗、载体疫苗以及溶瘤疱疹病毒等。
本研究得到了山东大学栾霁副研究员的支持,以及山东省自然科学基金、青岛市自然科学基金、山东大学杰出中青年学者基金和微生物技术研究院青年人才培育项目等项目的资助。
原文链接:
https://www.sciencedirect.com/science/article/pii/S2090123225010033